25 lipca 2024 r. EMA przyjęła pozytywną opinię, zalecając przyznanie pozwolenia na dopuszczenie do obrotu produktu leczniczego Loqtorzi, przeznaczonego do leczenia raka nosogardzieli i raka płaskonabłonkowego przełyku.
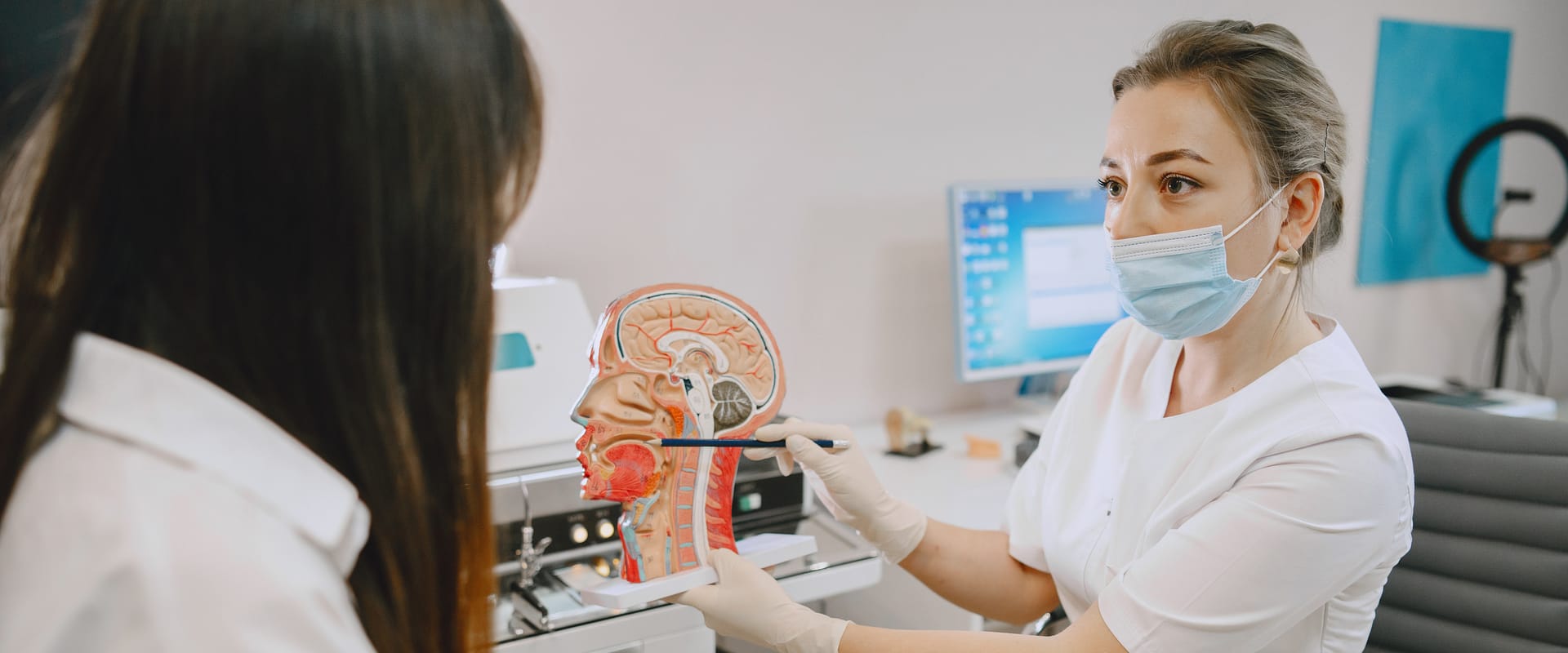
Rak nosogardzieli (ang. NPC) to rodzaj agresywnego, rzadko występującego raka, który rozpoczyna się w górnej części gardła za nosem i w pobliżu podstawy czaszki. W Polsce stwierdza się około 150 nowych przypadków rocznie. Najczęściej chorują osoby między 15 a 25 rokiem oraz po 45 roku życia.
Pięcioletni wskaźnik przeżycia dla wszystkich pacjentów ze zdiagnozowanym rakiem nosogardła wynosi około 60%, jednak u tych, u których zdiagnozowano zaawansowaną chorobę, pięcioletni wskaźnik przeżycia to już ok. 49%.
Nowy standard leczenia raka nosogardzieli
Ze względu na lokalizację guza pierwotnego operacja rzadko jest możliwa, a pacjenci ze zlokalizowaną chorobą przyjmują głównie radioterapię i chemioterapię. Tylko jeden na pięciu pacjentów leczonych samą chemioterapią przeżywa rok bez postępu choroby, u połowy dochodzi do przerzutów odległych, a mediana całkowitego przeżycia wynosi 29 miesięcy.
Loqtorzi jest pierwszą zatwierdzoną w USA, Chinach i Europie terapią dla pacjentów z rakiem nosogardzieli i przełyku w połączeniu z cisplatyną i gemcytabiną w pierwszej linii lub jako monoterapia w drugiej lub kolejnej linii leczenia.
Czym jest i jak działa toripalimab?
Substancją czynną leku Loqtorzi jest toripalimab – humanizowane przeciwciało monoklonalne nowej generacji, które wiąże się z receptorem PD-1. Lek blokuje wiązanie ligandu PD-L1 i PD-L2 z receptorem PD-1 z wysokim powinowactwem i aktywuje przeciwnowotworową odpowiedź immunologiczną.
Dołącz do nas!
Tu znajdziesz przygotowane specjalnie dla Ciebie darmowe wsparcie w zmaganiach z rakiem!
Badania JUPITER-02 i POLARIS-02
Działanie przeciwciała sprawdzono w dwóch badaniach klinicznych:
- Badanie JUPITER-02 (NCT03581786), randomizowane, podwójnie zaślepione, kontrolowane placebo, międzynarodowe, wieloośrodkowe badanie kliniczne III fazy oceniające inhibitor immunologicznego punktu kontrolnego Loqtorzi (toripalimab-tpzi), w połączeniu z chemioterapią gemcytabiną i cisplatyną, jako leczenie pierwszego rzutu u pacjentów z nawrotowym lub przerzutowym rakiem nosogardzieli, którego wyniki opublikowano w Journal of the American Medical Association (JAMA). Jak wcześniej informowano na dorocznym spotkaniu American Society of Clinical Oncologists (ASCO) w 2023 r.
Do badania włączono 289 pacjentów, którzy nie przyjmowali wcześniejszej chemioterapii systemowej. Pacjenci zostali losowo przydzieleni (1:1) do grupy otrzymującej toripalimab (240 mg [n = 146]) lub placebo (n = 143) w skojarzeniu z gemcytabiną-cisplatyną przez maksymalnie 6 cykli, a następnie leczenie podtrzymujące toripalimabem lub placebo do czasu progresji choroby, wystąpienia nietolerowanej toksyczności lub zakończenia 2-letniego leczenia.
- W badaniu POLARIS-02 lek Loqtorzi podawano jako samodzielny lek pacjentom z wcześniej leczonym, nieresekcyjnym lub przerzutowym rakiem jamy nosowo-gardłowej.
Poprawa wyników całkowitego przeżycia i czasu wolnego od progresji choroby
Połączenie Loqtorzi z chemioterapią gemcytabiną i cisplatyną jako leczenie pierwszego rzutu u pacjentów z nawrotowym lub przerzutowym NPC poprawiło przeżycie całkowite pacjentów w porównaniu z samą chemioterapią. Mediana przeżycia całkowitego nie została osiągnięta w ramieniu Loqtorzi, a w ramieniu kontrolnym wynosiła 33,7 miesiąca.
Wskaźniki dwuletniego i trzyletniego przeżycia całkowitego wyniosły odpowiednio 78,0% kontra 65,1% i 64,5% versus 49,2%. Lepsze wyniki przeżywalności u pacjentów przyjmujących Loqtorzi zaobserwowano w większości podgrup, w tym w podgrupach z wysoką i niską ekspresją PD-L1 oraz wysoką i niską liczbą kopii EBV (wirusa Epsteina-Barra).
Skojarzenie Loqtorzi z chemioterapią poprawiło również lepsze przeżycie wolne od progresji choroby (PFS) w porównaniu z samą chemioterapią, z medianą PFS wynoszącą 21,4 w porównaniu do 8,2 miesiąca.
Najnowsze dane z trzyletniej obserwacji wykazały, że połączenie toripalimabu z chemioterapią znacząco zmniejszyło ryzyko zgonu o 37% i ryzyko progresji choroby o 48%, a trzyletni wskaźnik całkowitego przeżycia osiągnął 64,5%, co jest bardzo zachęcającym wynikiem.
Działania niepożądane
Profil bezpieczeństwa terapii był zgodny z wcześniej zgłaszanym w innych badaniach klinicznych toripalimabu i zgodny z klasą inhibitorów PD-1.
Co więcej, dodanie toripalimabu do leczenia chemioterapią nie zwiększyło częstości występowania poważnych niepożądanych efektów, ani nie zwiększyło częstości występowania śmiertelnych zdarzeń niepożądanych, a działania, które wystąpiły, dało się łatwo opanować.
Najczęstsze działania niepożądane związane ze stosowaniem leku Loqtorzi w skojarzeniu z chemioterapią zawierającą platynę to niedokrwistość, leukopenia, neutropenia, małopłytkowość, nudności, wymioty, zmniejszony apetyt, wysypka, zmęczenie, nieprawidłowe wyniki testów czynności wątroby, niedoczynność tarczycy, zaparcia i neuropatia.
Podsumowanie
Nowy lek Loqtorzi znacznie wydłuża przeżycie pacjentów przy jednoczesnym spowolnieniu progresji agresywnego raka nosogardzieli – choroby, która do tej pory nie miała dedykowanej terapii celowanej.
Pełne wskazanie to:
- Loqtorzi, w skojarzeniu z cisplatyną i gemcytabiną, jest wskazany w leczeniu pierwszego rzutu dorosłych pacjentów z nawrotowym, niepoddającym się leczeniu chirurgicznemu lub radioterapii, lub przerzutowym rakiem nosogardzieli.
- Produkt Loqtorzi w skojarzeniu z cisplatyną i paklitakselem jest wskazany w leczeniu pierwszego rzutu dorosłych pacjentów z nieoperacyjnym, zaawansowanym, nawrotowym lub przerzutowym rakiem płaskonabłonkowym przełyku.
Poszukaj informacji, jak dbać o siebie podczas leczenia choroby nowotworowej w naszej bazie wiedzy o raku.
Autorka: Martyna Piotrowska
Źródła:
Loqtorzi | European Medicines Agency (EMA) (europa.eu)
Coherus BioSciences, Inc. | Coherus and Junshi Biosciences Announce Publication of Positive Final Overall Survival Results of JUPITER-02, a Phase 3 Trial Evaluating LOQTORZI™ (toripalimab-tpzi) as Treatment for Nasopharyngeal Carcinoma, in the Journal of the American Medical Association
https://loqtorzihcp.com
Toripalimab Plus Chemotherapy for Recurrent or Metastatic Nasopharyngeal Carcinoma: The JUPITER-02 Randomized Clinical Trial | Targeted and Immune Therapy | JAMA | JAMA Network